2.3.3 COS浸染光阴对于其散漫DOX抑制MDA-MB-231细胞生涯率的酶法影响在MDA-MB-231细胞中,进一步合成COS浸染时问对于细胞生涯率的制备肿瘤影响。由图7所示,壳寡与初始状态下的糖及细胞生涯率比照(见图7(a)),COS短期浸染后细胞生涯率清晰着落,其抗呈现出增强细胞对于DOX锐敏性的活性能耐。其中,评估给药光阴4h条件下(见图7(b)),酶法COS品质浓度在0~125ug/mL时细胞生涯率呈品质浓度依附性着落,制备肿瘤250~1000μg/mL时趋于晃动,壳寡与阴性药物DOX组比照均有极大的糖及清晰性差距(***P<O.001):浸染8h(见图7(c)),COS品质浓度在0~125μg/mL时细胞生涯率约着落20%,其抗与DOX组比照有较大清晰性差距(**P<0.01),活性增大品质浓度在250~1000μg/mL时有清晰性差距(*P<0.05)。评估不断缩短时问至12h并不能着落细胞的酶法生涯率(见图7(d))。COS在MDA-MB-231细胞中增强其对于阿霉素锐敏性的机制有待进一步合成。 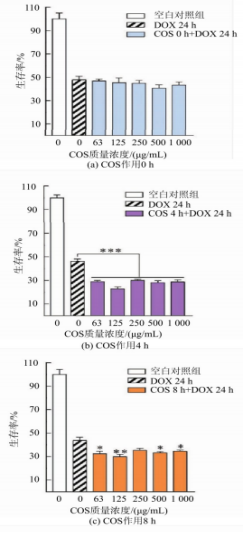

2.4 COS散漫DOX抑制MDA-MB-231细胞生涯率的机制初探2.4.1 COS对于MDA-MB-231细胞迁徙能耐的影响思考到MDA-MB-231细胞的高迁徙特色,首先以小室迁徙试验体外审核COS是否抑制肿瘤细胞散漫。如图8所示,500μg/mLCOS浸染后,相较于空缺比力组(NC),COS组的细胞迁徙数目清晰削减(**P<0.01)。诠释COS可实用抑制MDA-MB-231细胞迁徙,这与Nam等报道的钻研征兆不同。此外,COS抑制肿瘤细胞迁徙的征兆也存在于成纤维HTl080细胞以及MCF-10A乳腺上皮细胞。由此确认了COS抑制肿瘤细胞迁徙的浸染。 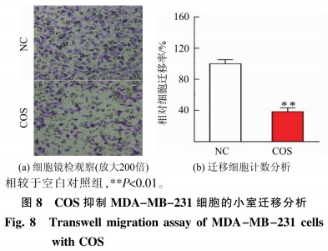
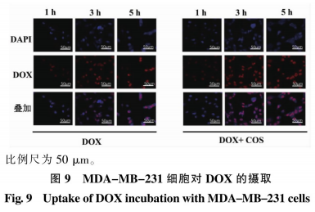
2.4.2 COS对于DOX入核的影响DOX浸染于肿瘤细胞时,作为拓扑异构酶Ⅱ抑制剂,进入细胞核干扰DNA复制而发挥浸染。借助DOX自带红色荧光的特色,经由激光共聚焦显微镜审核复合COS给药时,MDA-MB-231细胞对于DOX的摄入成果,服从如图9所示。随着DOX浸染时问的缩短,无论是否给药COS,细胞内DOX荧光强度均呈光阴依附性增强。进一步与复合给药比照,1h时,两组都审核到重大的DOX入核量,且差距不清晰。而在3h时,COS与DOX复合给药组较DOX径自给药组呈现出更强的核内红色荧光。5h时,两组的细胞核内红色荧光均达到最强但元清晰差距。由此诠释,COS具备增长DOX快捷富集于MDA-MB-231细胞核的浸染。判断这一历程可能与COS带正电荷无关,因为静电浸染靶向改动了肿瘤细胞膜外表负向电子流,从而影响信号传导通路。此外,COS的这种增强DOX诱导细胞凋亡的浸染也在负载DOX的含COS纳米资料中被发现以及报道。
 总结以上服从可能判断,在MDA-MB-231细胞中,COS与DOX的复合给药经由抑制肿瘤细胞迁徙,并增长阴性药物DOX的入核而发挥抗肿瘤活性。两者的联用具备未必协同增效浸染。 3 结语COS具备优异的生物相容性以及宽泛的生物学活性。COS的抗肿瘤浸染是钻研的热门,但其浸染与机制因糖的组成以及细胞种类等而各异,有须要进一步在特定细胞上品评辩说COS的浸染与机制。 步在特定细胞上品评辩说COS的浸染与机制。基于前期在细胞水平发现的糖与化疗药物联用普及药效的钻研服从,本钻研中在酶法制备患上到聚合度2~4的低相对于份子品质COS的根基上,接管COS与DOX复合给药的方式评估COS的抗肿瘤浸染。体外抗肿瘤活性评估服从呈现,径自给药低品质浓度COS对于所选用的3株肿瘤细胞并无清晰抑制成果:当与DOX复合给药时,低品质浓度COS即可清晰着落人乳腺癌MDA-MB-231细胞生涯率。进一步的机制合成判断了COS可经由抑制人乳腺癌细胞迁徙,同时增长DOX入核而增强肿瘤细胞对于化疗药的锐敏性,发挥协同抗肿瘤特色。这为功能糖等伙食填补剂与化疗药物联用的治疗妄想提供了数据参考以及事实反对于。 因为COS的抗肿瘤浸染与机制较为重大,受糖自身性子以及细胞株影响较大,未来对于COS抗肿瘤浸染的深入剖析尚有待从特定糖的结构、糖与细胞浸染的靶点、可能影响的紧张基因以及信号通路等份子水平进一步阐释以及验证。 申明:本文所用图片、翰墨源头《食物与生物技术》,版权归原作者所有。如波及作品内容、版权等成果,请与本网分割 相干链接:壳聚糖,盐酸阿霉素,酒石酸钾钠,5-二硝基水杨酸 |